那娜教授课题组:轴向配位非对称局域电场增强酶催化协同治疗
文章来源:北京师范大学化学学院,发布时间:2026-04-03
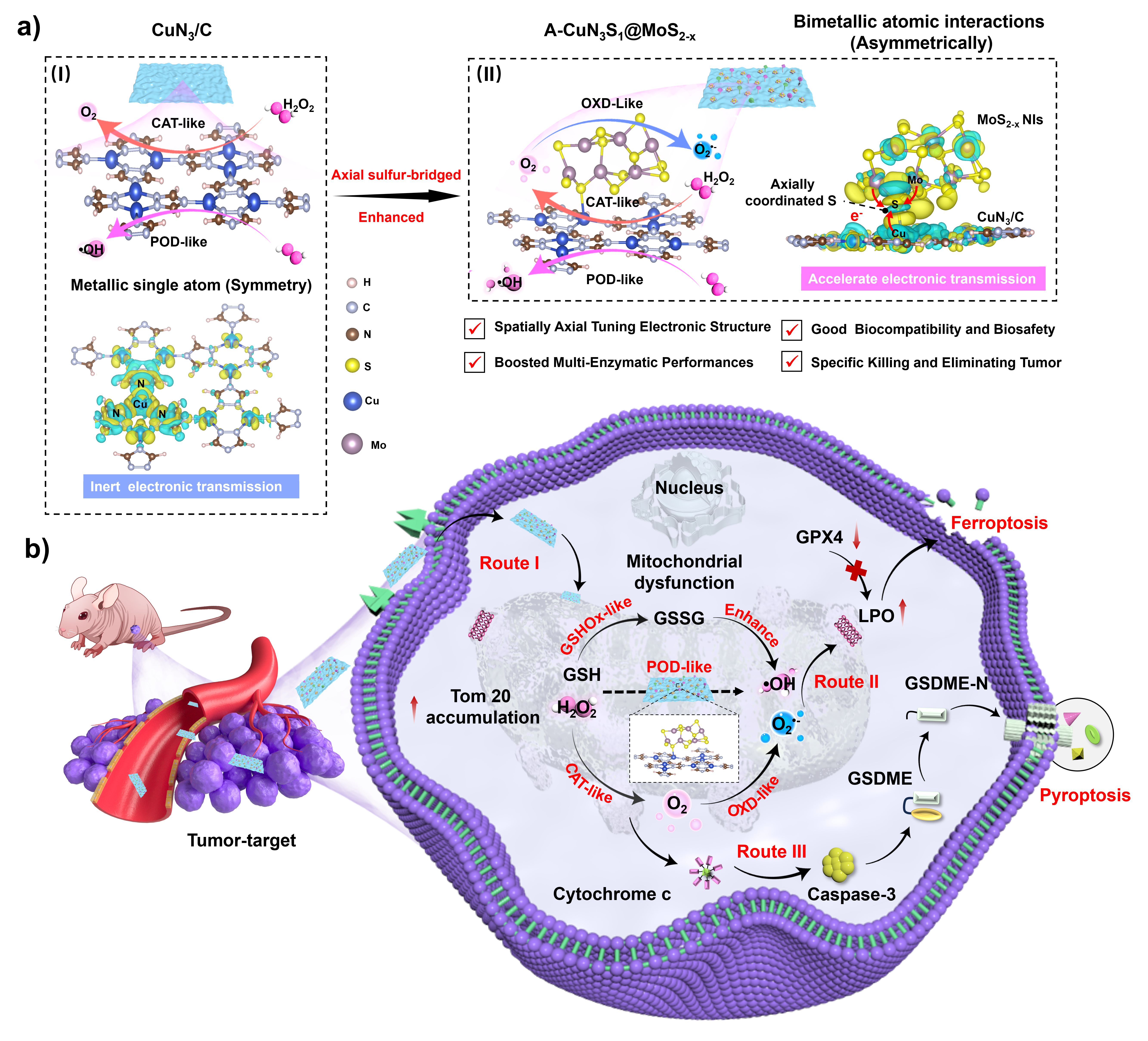
近年来,纳米酶在活性氧(ROS)介导的铁死亡、焦亡等非凋亡性细胞死亡调控中展现出广阔的应用前景,但其催化性能一定程度仍受限于金属活性中心单一配位模式所导致的相邻原子有限局域电场,一定程度上限制了肿瘤治疗效率的进一步提升。针对这一问题,北京师范大学化学学院那娜教授课题组创新性地采用纳米岛(NIs)介导的轴向配体桥接策略,成功构建了一种具有非对称局域电场(LEF)的轴向硫桥连Mo-S-Cu纳米酶(A-CuN3S1@MoS2-x),实现了铁死亡-焦亡联合治疗,显著增强了癌症治疗效果。该纳米酶结构中,CuN3/C纳米片表面的Cu原子与纳米岛中的Mo位点通过硫(S)桥实现轴向连接,形成独特的非对称局域电场,这一结构可有效加速纳米酶与底物之间的电子转移效率,进而精准调控其多酶催化活性。理论计算结果进一步证实,S桥的引入可诱导Cu-N3纵向轴向上产生非对称电子分布,从而大幅提升纳米酶的过氧化氢酶及过氧化物酶活性。与此同时,Mo
文章来源:北京师范大学化学学院,发布时间:2026-04-03
近年来,纳米酶在活性氧(ROS)介导的铁死亡、焦亡等非凋亡性细胞死亡调控中展现出广阔的应用前景,但其催化性能一定程度仍受限于金属活性中心单一配位模式所导致的相邻原子有限局域电场,一定程度上限制了肿瘤治疗效率的进一步提升。针对这一问题,北京师范大学化学学院那娜教授课题组创新性地采用纳米岛(NIs)介导的轴向配体桥接策略,成功构建了一种具有非对称局域电场(LEF)的轴向硫桥连Mo-S-Cu纳米酶(A-CuN3S1@MoS2-x),实现了铁死亡-焦亡联合治疗,显著增强了癌症治疗效果。该纳米酶结构中,CuN3/C纳米片表面的Cu原子与纳米岛中的Mo位点通过硫(S)桥实现轴向连接,形成独特的非对称局域电场,这一结构可有效加速纳米酶与底物之间的电子转移效率,进而精准调控其多酶催化活性。理论计算结果进一步证实,S桥的引入可诱导Cu-N3纵向轴向上产生非对称电子分布,从而大幅提升纳米酶的过氧化氢酶及过氧化物酶活性。与此同时,Mo